①物質の変化と種類
📌はじめに
おそらく文系出身者は、この化学の分野でつまずくかもしれません。
正直私は、化学は最後まで得意にはなりませんでした。
でも、よく出るポイントだけ押さえたことで
本試験では「捨て問」と割り切れるようになり、
気持ちがかなり楽になりました。
私の場合、全部理解しようとするのをやめ、「乙4は6割取れればいい」と割り切って、化学は次の3つだけに絞りました。
・燃えやすいかどうか
・水に溶けるか
・引火点が低いか
この分野では、項目💬 初学者と運営者のミニ対話をおススメします。

🔹 1. 化学変化(化学反応)って何?
化学変化は、物質の性質が変わり、新しい物質ができる変化 です。
たとえば…
✔ 鉄がさびる
鉄(Fe)+ 酸素(O₂) → 酸化鉄(Fe₂O₃)
→ 元の鉄とは性質の違う物質ができています。
✔ 水素と酸素が反応して水になる
2H₂ + O₂ → 2H₂O
→ 気体同士から別の液体が生成されています。
🔹 2. 化学変化と物理変化との違い
比較して覚えると理解が早いです:
| 変化の種類 | 何が変わる? | 物質はどうなる? |
|---|---|---|
| 物理変化 | 状態・形など | 元の物質のまま(例:水の氷結) |
| 化学変化 | 性質・組成 | 新しい物質ができる(例:水ができる) |
👉 試験では
「物質が新しくできたかどうか」 で判断すると正解しやすいです。
🔹 3. 物理・物理変化の種類(試験でよく出る)
物理変化は形状・形態が変わるだけの変化をいう。
これに対し、化学変化はある物質が別の物質に変化し元々もっていた性質が変化する現象をいう。
- 化合:2種類以上の物質が結びついて新しい物質になる。
- 酸化:物質が酸素と化合すること(酸化は化合の一つ)
- 分解:1つの物質が2種類以上の物質に分かれる
などがある。
| 物理変化の具体例 |
| 水が冷えて氷になる(凝固) |
| ドライアイスが二酸化炭素になる(昇華) |
| 水とアルコールを混ぜる(混合) |
| 金属を加熱すると膨張する(体積の変化) |
| バネに力を加えて伸ばす(変形) |
| 化学変化の具体例 |
| 鉄が空気中で酸素と反応して酸化鉄(錆)になる。(酸化) |
| 木材やガソリンなどが酸素と反応して熱や光を出す反応(燃焼) |
| 水に電気を流すと、水素と酸素に分解される反応(電気分解) |
🔹 4. 物質の分類
物質は性質によって次のように分けられます:
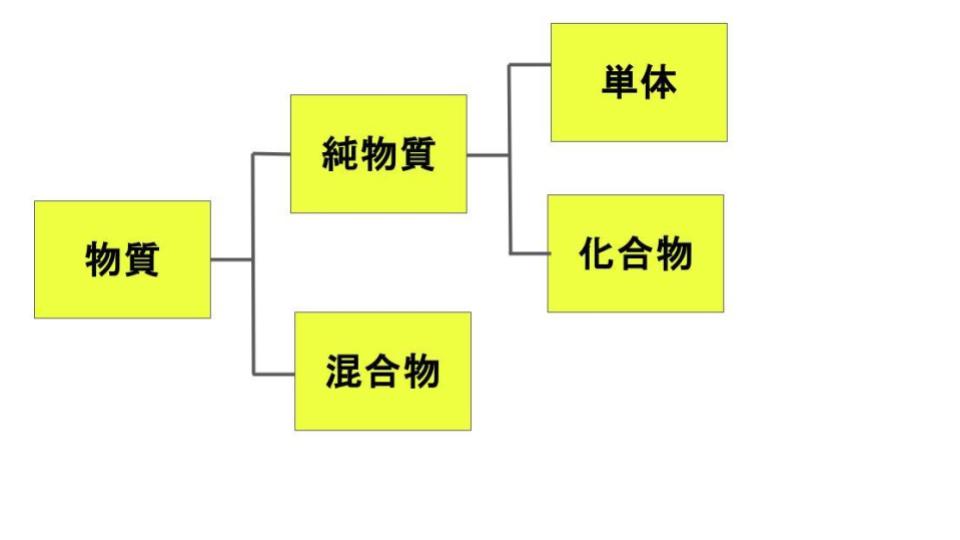
1. 純物質
→ 1種類の成分だけで構成された物質
・単体:1種類の元素だけ(例:酸素、炭素)
・化合物:複数の元素が結合(例:水 CO₂)
2. 混合物
→ 複数の純物質がただ混ざっているだけのもの
例:空気、食塩水、石油など
🔹 同素体と異性体
- 同素体 → 同じ元素からできているのに性質が違う物質
例:炭素からできる ダイヤモンド と 黒鉛(グラファイト) - 異性体 → 同じ分子式でも構造が違って性質が違う化合物
例:C₂H₆O の異性体(エタノール vs ジメチルエーテル)
👉 乙4では
「名前を聞いたことがある」程度でOKです。
たとえば、ダイヤモンドと黒鉛(鉛筆の芯)はどちらも、炭素「C」という元素でできた単体だが、性質は違うので同素体である。
ダイヤモンドは固いが、黒鉛はもろい。
他にも同素体・・・
| 元素 | 硫黄S | 炭素C | 酸素O | リンP |
| 同素体 | 斜方硫黄 単斜硫黄 ゴム状硫黄 | ダイヤモンド 黒鉛 | 酸素 オゾン | 黄リン 赤リン |
覚え方の例として元素記号をとって、「同素体はSCOP(スコップ)」と語呂合わせで覚えるといいです。
いいですね 👍
乙4はここ“超頻出”です。
そのまま使える簡潔版👇
📌 “判断フロー”で覚える
1️⃣ 新しい物質ができている?
- できる → 👉 化学変化
- できない → 👉 物理変化
2️⃣ 状態が変わっただけ?
(氷→水、蒸発など)
→ 👉 物理変化
3️⃣ 発熱・発光・沈殿・気体発生ある?
→ 👉 化学変化
❌ “運営者が間違えた思考パターン”3選
私(運営者)の失敗例を紹介します。
🚫 NG①: 「見た目が変わった=化学変化」と思った
→ ❌ 氷が溶ける=化学変化?
→ ⭕ 新しい物質はできていない=物理変化
🚫 NG②: 「気体が出た=物理変化」と思った
→ ❌ 泡が出ただけ?
→ ⭕ 気体発生は基本 化学変化
🚫 NG③: 「燃える=ただ溶ける」と思った
→ ❌ 形が変わっただけ?
→ ⭕ 燃焼は新しい物質ができる=化学変化
📝 5. まとめ
- 🔥 化学変化 は物質が別の物質に変わる変化。
- 💧 物理変化 は物質自体は変わらず、形や状態だけが変化。
- 📦 純物質:1種類の成分からできている物質(単体 or 化合物)。
- 🧪 混合物:複数の純物質が混ざっているだけのもの(性質は混ざるだけ)。
- 🔁 同素体:同じ元素でも結びつき方が違って性質が異なる物質。
💬 初学者と運営者のミニ対話
初学者
化学変化ってよく聞くけど、結局何が起きてるの?🤔
運営者
簡単にいうと、ある物質が別の物質に変わる変化のことだよ。性質そのものが変わって、元の物質に戻らない場合が多いんだ。
初学者
じゃあ氷が溶けるのは化学変化なの?😳
運営者
それは 物理変化 っていうよ。見た目や状態が変わるだけで、物質そのもの(H₂O)が変わっていないからね。
初学者
なるほど〜✍️
でも「物質の種類」ってどうやって区別するの?🤨
運営者
物質は大きく
純物質(成分が1つだけ)
混合物(複数の純物質が混ざっている)
に分けられるよ。
初学者
純物質の中でもいろいろあるんだよね?😅
運営者
そう!純物質は
単体(元素1種類だけ)
化合物(2種類以上の元素が結びついたもの)
って分け方をするよ。たとえば、水は化合物、酸素(O₂)は単体だね。
初学者
同じ元素でも違う性質になるのってある?😯
運営者
あるよ!それが 同素体。
たとえば ダイヤモンドと黒鉛 はどちらも炭素だけど性質が違うんだ。


コメント